纳米酶是一类可模拟生物酶催化活性的纳米材料,具有很多天然酶不可比拟的优势,在生物分析、疾病诊断和治疗等领域表现出重要应用前景。至今,已有数百种纳米材料被报道出具有类酶催化特征。其中,金属纳米酶因其明确、稳定、可调控的物化结构,以及经常表现多类酶活性特点,已成为纳米酶家族的重要成员。纳米催化材料与应用团队入选2018年度河南省高校科技创新团队,聚焦纳米催化材料及其催化机制方面的研究,开发了一些贵金属基纳米酶材料并探索它们在生物检测和生物保护方面的潜在应用。下面是该团队近期在贵金属纳米酶催化领域取得的一些研究进展。
生命是一种动态平衡体。平衡状态的打破将会导致生理功能的缺陷,进而威胁生命健康。氧化应激是体内氧化与抗氧化作用失衡的一种状态,被认为是导致衰老和很多重要疾病的重要因素之一。贵金属纳米酶具有的类酶多样性特征,可以在生物体内表现出复杂的抗氧化与促氧化活性,能对氧化应激起到重要调节作用,有利于其发挥独特生物学功能。结合前期工作基础,何伟伟课题组通过改变化学组成实现了对贵金属纳米酶抗氧化与促氧化活性的共同调节。他们利用简单的化学方法,合成了一系列组分可调的PtRu合金纳米颗粒。在接下来的实验中他们证明了PtRu 纳米颗粒表现出多种类酶催化活性(包括过氧化物酶,氧化酶,亚铁氧化物酶,过氧化氢酶和超氧化物歧化酶)和1,1-二苯基-2-吡啶基肼基自由基清除活性。PtRu纳米酶表现出促氧化和抗氧化双功能:一方面可以催化有机底物分子和金属离子的氧化,另一方面能够有效清除自由基和活分子。PtRu纳米颗粒的多种类酶催化活性均高度依赖于Pt/Ru合金比例,并且随着组分的变化,其抗氧化能力和促氧化能力显示出相同的变化趋势。在合适的比例下,PtRu合金化可以同时增强抗氧化和促氧化活性。基于过氧化氢模拟酶的活性,他们尝试将PtRu纳米酶用于保护天然活性产物(红曲色素)免受氧化分解,发现具有很好的保护效果。该研究可为优化纳米酶的抗氧化和促氧化能力提供依据,可为纳米酶在保护具有生物活性的天然产物应用提供借鉴,同时也为生物环境中氧化应激水平的调节提供一些思考。该研究成果以“Regulating the pro- and anti-oxidant capabilities of bimetallic nanozymes for the detection of Fe2+ and protection of Monascuspigments”为题发表于《Nanoscale》,刘闯同学为论文第一作者(Nanoscale, 2020, 12, 3068)。
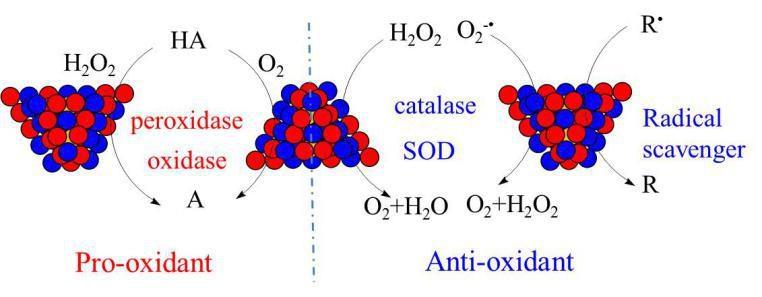
图1:PtRu合金纳米酶抗氧化与促氧化机理图
PtCu纳米酶清除ROS阻止病理性α突触核蛋白传播用于帕金森病治疗
帕金森病(Parkinson’s disease,PD),是最常见的神经退行性疾病之一,多发于老年人,我国65岁以上人群PD的患病率大约是1.7%。帕金森病特征是路易体中的 α-突触核蛋白(α-synuclein)异常聚集和积累。尽管一些帕金森病例与家族性PD相关,但大多数病例是散发性,至今确切病因不明,尚无有效的治疗和预防办法。近年来,德国著名学者Braak提出的分期理论颠覆了学界对PD的认知。该理论认为,病理性α-突触核蛋白是一种类似病毒的蛋白,在PD大脑中可从一个区域传播到另一个区域,从而加重PD病理演化。许多新的研究表明,氧化应激水平升高是导致病毒样α-突触核蛋白扩散的关键诱因。那么,如果找到一种能够有效降低氧化应激水平且生物兼容性好的纳米材料,可能会抑制病理性α-突触核蛋白的扩散,无疑会对减轻PD发病具有重要作用。
针对这一问题,何伟伟课题组与美国约翰斯·霍普金斯大学医学院毛晓波教授、清华大学化学系李艳梅教授合作,设计了一种具有良好生物兼容性的PtCu合金纳米酶。抗氧化实验表明,PtCu纳米酶具有类过氧化氢酶、类过氧化物酶和类超氧化物歧化酶等多重模拟酶活性以及清除自由基的能力,这使PtCu纳米颗粒成为抑制活性氧物种产生的抗氧化剂。为了评价PtCu纳米颗粒在体外和体内的生物活性,他们建立了α-突触核蛋白预制纤维体(PFF)诱导的帕金森疾病模型。体外细胞实验表明在神经元细胞培养物中添加PFF会引起ROS水平提高,α-突触核蛋白积聚,呈现出病理性和神经毒性,而PtCu纳米酶能显著减少由PFF诱导引起的ROS水平升高,降低α-突触核蛋白病理性和神经毒性,更为重要的是PtCu纳米酶能阻断病理性α-突触核蛋白在细胞间的传播。基于细胞实验结果,构建了小鼠散发性PD模型,体内实验表明经PtCu纳米酶处理能显著抑制了α-突触核蛋白从纹状体向黑质的扩散。为纳米酶在PD疾病治疗中的应用提供了新策略。该研究关于纳米酶在阻止α-突触核蛋白的应用有望为阿尔茨海默病等其他神经退行性病变治疗和预防提供参考。相关研究成果以“Nanozyme scavenging ROS for prevention of pathologic α-synuclein transmission in Parkinson’s disease”为题发表于《Nano Today》(Nano Today,2021, 36, 101027.),我校2015级本科生毛远洋(现为河南大学研究生,指导老师何伟伟)和清华大学博士刘雨青为该论文的共同第一作者。

图2:PtCu纳米酶清除活性氧物种和阻止病理α-突触核蛋白细胞间传播示意图
多酶活性增强的三金属PtPdCu纳米材料用于Fe2+检测及抗氧化效应
纳米酶的应用不仅决定于模拟酶种类,而且还决定于催化效率。目前,发现新种类模拟酶困难很大,然而对纳米酶催化活性的提高和优化却有很大的研究空间。特别是在调节纳米颗粒理化参数来获得较高类酶催化活性方面,国内外同行做了大量的探索性工作。基于前期在双金属纳米酶活性组分调控的研究,何伟伟课题组发现三金属纳米结构得益于杂原子之间的协同效应能够表现出更强的类酶催化活性(ACS Appl. Nano Mater., 2018, 1, 222–231.)。最近,他们又将Cu元素引入到PtPd合金,制备了一种表面富Pt的非均相PtPdCu合金纳米颗粒(Pt总含量为16%)。受益于这种独特结构,PtPdCu合金颗粒相与PtPd纳米颗粒和商业Pt/C催化剂相比,表现出显著增强的类酶催化活性(包括过氧化物酶、亚铁氧化酶、过氧化氢酶)和1,1-二苯基-2-三硝基苯肼(DPPH)自由基清除能力。与报道的一些类过氧化氢纳米颗粒相比,PtPdCu合金颗粒拥有最高的最大反应速率(5.7×104 µM min-1)。PtPdCu 优良的类铁氧化酶特征可用于Fe2+的检测,该方法选择性高、灵敏度高且准确度好,可用于补铁口服液中Fe含量的测定。基于抗氧化分子对PtPdCu类过氧化物酶活性的抑制作用,PtPdCu纳米酶还可用于抗氧化能力分析。他们发现三种天然抗氧化剂单宁酸(TA),没食子酸(GA)和抗坏血酸(AA)对PtPdCu的过氧化物酶活性表现出截然不同的抑制行为和抗氧化能力(TA > GA > AA)。基于此原理,他们还进一步探索了该纳米材料用于四种绿茶提取物(毛尖、龙井、铁观音和茉莉花茶)的抗氧化水平研究。该工作可为抗氧化能力评价、纳米酶与抗氧化剂相互作用研究提供参考。另外,PtPdCu纳米酶优异的过氧化氢酶活性和自由基清除活性也有望在生物保护中发挥作用。相关研究成果以“Enhanced Multiple Enzymelike Activity of PtPdCu Trimetallic Nanostructures for Detection of Fe2+ and Evaluation of Antioxidant Capability”为题发表于《ACS Sustainable Chem. Eng.》(ACS Sustainable Chem. Eng., 2020, DOI: 10.1021/acssuschemeng.0c08230.),毛远洋为该论文的第一作者。
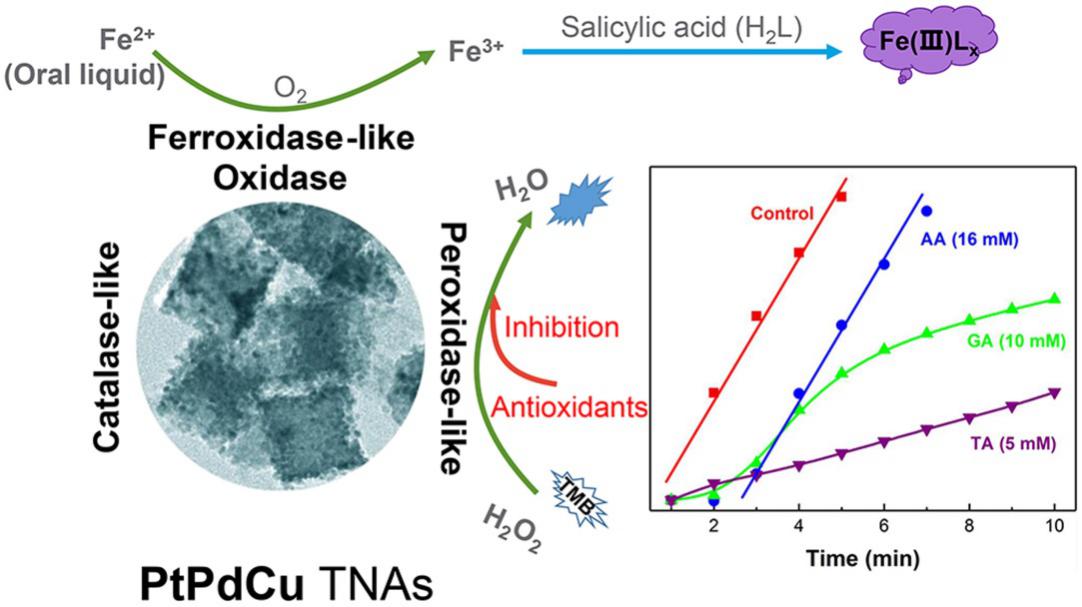
图3:PtPdCu纳米酶可用于Fe2+检测和抗氧化能力评估
以上研究得到了国家自然科学基金、河南省高层次人才特殊支持计划(中原千人计划)、河南省高校科技创新团队等项目的支持。